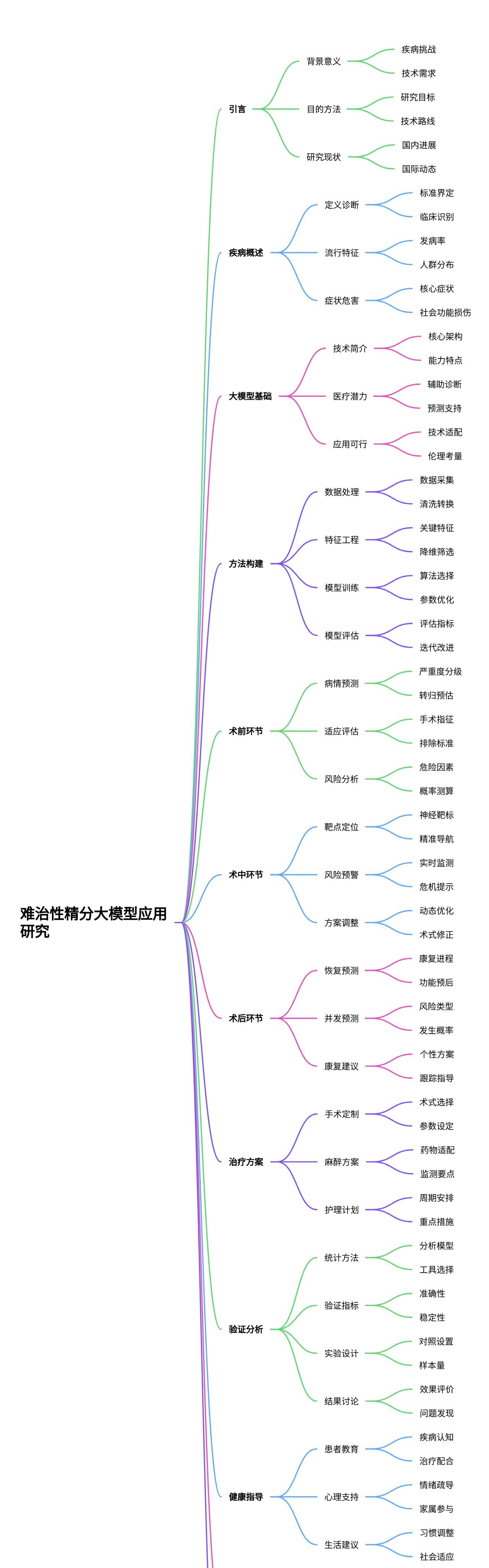
目录
一、引言
1.1 研究背景与意义
1.2 研究目的与方法
1.3 国内外研究现状
二、难治性精神分裂症概述
2.1 定义与诊断标准
2.2 流行病学特征
2.3 临床症状与危害
三、大模型技术原理与应用基础
3.1 大模型简介
3.2 在医疗领域的应用潜力
3.3 应用于难治性精神分裂症的可行性
四、大模型预测难治性精神分裂症的方法与模型构建
4.1 数据收集与预处理
4.2 特征工程
4.3 模型选择与训练
4.4 模型评估与优化
五、术前预测与评估
5.1 病情严重程度预测
5.2 手术适应症评估
5.3 风险因素分析
六、术中监测与辅助决策
6.1 手术靶点定位
6.2 实时风险预警
6.3 手术方案调整
七、术后恢复与并发症预测
7.1 恢复情况预测
7.2 并发症风险预测
7.3 个性化康复建议
八、基于预测结果的治疗方案制定
8.1 手术方案定制
8.2 麻醉方案选择
8.3 术后护理计划
九、统计分析与技术验证
9.1 统计方法选择
9.2 模型验证指标
9.3 实验验证设计
9.4 结果分析与讨论
十、健康教育与指导
10.1 患者及家属教育
10.2 康复期心理支持
10.3 生活方式建议
十一、案例分析
11.1 成功案例展示
11.2 经验总结与启示
11.3 失败案例反思
十二、研究结论与展望
12.1 研究成果总结
12.2 研究的局限性
12.3 未来研究方向
一、引言
1.1 研究背景与意义
难治性精神分裂症(Treatment-Resistant Schizophrenia,TRS)是精神科领域极具挑战性的难题。据统计,约 25%-30% 的精神分裂症患者属于难治性,其特征为对常规抗精神病药物治疗反应不佳,症状难以有效缓解。这些患者不仅面临着严重的精神病理症状,如幻觉、妄想、思维紊乱等,还在社会心理功能、生活质量等方面遭受极大影响,给家庭和社会带来沉重负担。传统治疗手段在应对 TRS 时存在诸多局限性,药物治疗效果有限,且易引发患者无法耐受的不良反应,如锥体外系反应、代谢综合征等。手术治疗虽为部分患者带来希望,但手术风险、术后并发症以及个体差异导致的疗效不确定性,使得手术方案的制定和实施充满挑战。
随着人工智能技术的飞速发展,大模型在医疗领域的应用逐渐展现出巨大潜力。大模型凭借其强大的数据处理和分析能力,能够整合多源信息,挖掘数据间的潜在关联,为 TRS 的预测和治疗提供全新视角。通过对患者临床特征、基因信息、神经影像等多模态数据的学习,大模型有望实现对 TRS 术前、术中、术后情况以及并发症风险的精准预测,从而为制定个性化的手术方案、麻醉方案和术后护理计划提供科学依据,提高治疗效果,改善患者预后。将大模型应用于 TRS 的研究,不仅是对精神医学治疗手段的创新探索,更是满足临床需求、提升患者生活质量的迫切需要,对于推动精神医学领域的发展具有重要的现实意义。
1.2 研究目的与方法
本研究旨在利用大模型提升难治性精神分裂症的预测和治疗水平,通过对患者多模态数据的分析,实现对手术各阶段及并发症风险的准确预测,并依据预测结果制定优化的治疗方案,包括手术方案、麻醉方案和术后护理计划等,以提高治疗效果,改善患者的生活质量和社会功能。
在研究方法上,本研究采用了文献研究法,全面梳理国内外相关文献,了解大模型在精神疾病领域尤其是难治性精神分裂症治疗中的研究现状、应用进展及存在问题,为研究提供理论基础和思路借鉴。同时,运用案例分析法,收集临床中难治性精神分裂症患者的详细病例资料,包括患者的基本信息、病史、症状表现、治疗过程及结果等,运用大模型对这些案例数据进行分析,验证模型的预测能力和治疗方案的有效性,并通过实际案例不断优化模型和治疗方案。此外,还结合了数据挖掘和机器学习技术,对大量的临床数据进行预处理、特征提取和模型训练,构建适用于难治性精神分裂症预测和治疗的大模型,通过交叉验证、准确率、召回率等指标评估模型性能,确保模型的可靠性和准确性。
1.3 国内外研究现状
在国外,大模型在精神疾病领域的研究和应用已取得一定进展。部分研究利用大模型对精神分裂症的症状进行分析和预测,通过自然语言处理技术分析患者的文本描述,识别潜在的症状线索,辅助诊断和病情评估。在治疗方面,有研究尝试运用大模型制定个性化的治疗方案,根据患者的基因数据、临床特征等信息,预测不同治疗方法的疗效,为医生提供治疗决策支持。例如,[具体研究名称] 通过对大量精神分裂症患者数据的学习,建立了基于深度学习的治疗推荐模型,能够根据患者个体情况推荐最适合的药物和治疗剂量,取得了较好的初步效果。然而,这些研究在应用于难治性精神分裂症时仍存在不足。由于难治性精神分裂症的复杂性和异质性,现有的模型在预测精度和泛化能力上有待提高,对于手术相关的预测和治疗方案制定的研究相对较少,缺乏全面、系统的解决方案。
在国内,大模型在精神医学领域的研究也逐渐受到关注。一些研究聚焦于利用大模型辅助精神疾病的诊断,通过整合临床数据和影像信息,提高诊断的准确性和效率。针对难治性精神分裂症,部分研究尝试结合中医理论和人工智能技术,探索新的治疗思路和方法。但整体而言,国内的研究仍处于起步阶段,在模型的构建和优化、临床应用的验证等方面还需要进一步深入探索。现有研究多集中在单一模态数据的分析,缺乏对多模态数据融合的有效方法,难以充分挖掘数据背后的信息,影响了模型的性能和应用效果。
二、难治性精神分裂症概述
2.1 定义与诊断标准
难治性精神分裂症,是精神分裂症中治疗较为棘手的一类亚型,其定义在国际和国内的医学领域逐渐达成相对统一的共识。从国际视角来看,2017 年精神病治疗应答及抵抗(TRRIP)工作组在国际专家共识基础上,将难治性精神分裂症(TRS)定义为至少具有中度症状严重程度和精神分裂症所致功能障碍,且对 2 次或 2 次以上抗精神病药物试验应答不充分。每次抗精神病药物试验需满足足够剂量(相当于每天至少服用 600 毫克氯丙嗪)、持续时间(至少 6 周)以及患者依从性(至少服用处方剂量的 80%) 。最佳 TRRIP 标准还涵盖通过量表对症状严重程度进行前瞻性监测,确认在抗精神病药物治疗过程中症状减少少于 20%,并通过 2 个或更多血浆水平确认抗精神病药物的依从性,以及试用至少一种长效注射剂。美国的疾病分类和诊断统计手册 DSM-Ⅳ-TR 也对精神分裂症的诊断标准做出明确界定,虽未单独详述难治性精神分裂症,但为诊断提供了基础框架,在病程、症状表现等方面的规定,为难治性精神分裂症的诊断提供参考。
在国内,常用的诊断标准为中国精神障碍分类与诊断标准 CCMD-3。其中有关难治性精神分裂症的概念为,按通常方法进行治疗而不能获得理想疗效的一群患者,具体包含过去 5 年对 3 种药物剂量和疗程适当的抗精神病药物(3 种中至少有 2 种化学结构是不同的)治疗反应不佳;或不能耐受抗精神病药物的不良反应;或即使有充分的维持治疗或预防治疗,病情仍然复发或恶化的患者。部分专家学者也提出药物治疗时间 12 周,治疗剂量可根据是否达到有效血药浓度、是否达常规有效剂量来判断,既往使用药物种数,可按系统观察两个不同化学结构的药物处理,进一步细化诊断考量因素 。
2.2 流行病学特征
从全球范围来看,精神分裂症的年发病率为 7‰ – 14‰,而其中难治性精神分裂症占比约 25%-30%。在不同国家和地区,其患病率和发病率存在一定差异。在欧美一些发达国家,由于精神卫生服务体系相对完善,统计数据相对准确,难治性精神分裂症的患病率约在 1.5%-2% 之间,且发病率呈相对稳定态势。在亚洲部分国家,由于人口基数大、精神卫生资源分布不均等因素,虽确切患病率难以精准统计,但临床数据显示,其患病率和发病率均不容小觑,且有上升趋势。在非洲等医疗卫生条件相对落后的地区,由于诊断水平有限、患者就诊率低等原因,相关数据统计存在较大误差,但可以推测,在这些地区,由于缺乏及时有效的治疗,精神分裂症发展为难治性的比例可能更高。
在国内,随着精神卫生事业的发展和对精神疾病的重视程度提高,对难治性精神分裂症的流行病学研究逐渐增多。国内研究表明,难治性精神分裂症在精神分裂症患者中的占比与国际水平相近。在经济发达的东部沿海地区,由于医疗资源丰富,患者能够得到及时诊断和治疗,患病率相对稳定;而在中西部一些经济欠发达地区,由于医疗资源相对匮乏,患者就诊延迟,导致患病率相对较高,且发病率呈上升趋势。
高危因素方面,家族遗传因素在难治性精神分裂症的发病中起到重要作用。研究表明,若家族中有精神分裂症患者,尤其是直系亲属患病,其后代患难治性精神分裂症的风险显著增加。患者的首发年龄也是关键因素,首发年龄越小,发展为难治性精神分裂症的可能性越大,这可能与青少年时期大脑发育尚未成熟,对精神刺激的耐受性较低有关。长期未接受有效治疗或治疗不规范,导致病情迁延不愈,也是发展为难治性的重要原因。患者的生活环境和社会支持系统同样影响发病风险,长期处于应激状态、生活压力大、缺乏社会支持的患者,更容易发展为难治性精神分裂症 。
2.3 临床症状与危害
难治性精神分裂症的临床症状复杂多样,常见症状包括幻觉、妄想、思维混乱、情感淡漠、意志减退等。幻觉以幻听最为常见,患者常常听到不存在的声音,如听到有人议论自己、辱骂自己,这些声音严重干扰患者的思维和行为;妄想则表现为被害妄想、关系妄想、夸大妄想等,患者坚信自己受到迫害、与周围事物存在特殊关联或拥有非凡能力,如认为有人在食物中下药谋害自己、将周围人的正常行为解读为针对自己的阴谋等。思维混乱表现为言语逻辑紊乱、话题跳跃,患者难以清晰表达自己的想法,交流困难;情感淡漠使患者对周围事物缺乏情感反应,对亲人朋友的关心无动于衷,面部表情呆滞;意志减退导致患者生活懒散,缺乏主动性和进取心,对工作、学习和社交活动失去兴趣,甚至日常生活自理能力下降。
这些症状对患者的身心健康造成严重危害,使患者长期处于痛苦和恐惧之中,生活质量急剧下降,无法正常工作、学习和社交,自我认知和自尊心受到极大打击,部分患者还会出现自伤、自杀等极端行为,严重威胁自身生命安全。对患者家庭而言,不仅要承担巨大的经济负担,包括长期的医疗费用、照顾患者的人力成本等,家庭成员的心理也承受着沉重压力,生活受到严重影响,家庭关系变得紧张。从社会层面看,难治性精神分裂症患者由于行为异常,可能对他人和社会秩序造成威胁,增加社会不安定因素,同时也给社会医疗资源、福利保障体系带来沉重负担,阻碍社会的和谐发展 。
三、大模型技术原理与应用基础
3.1 大模型简介
大模型,作为人工智能领域的关键技术,指的是具有庞大参数规模和复杂计算结构的机器学习模型,通常基于深度神经网络构建,其参数数量可达数十亿甚至数千亿级别。这些模型通过在海量数据上进行训练,能够学习到丰富的数据模式和知识,具备强大的表达能力和泛化能力,可执行多种复杂任务。
大模型的发展历程是一部充满创新与突破的历史。早期,传统机器学习模型如支持向量机(SVM)、决策树等在解决特定问题时发挥了重要作用,但随着数据量的爆发式增长和对模型性能要求的不断提高,这些模型逐渐显露出局限性。21 世纪初,深度学习技术的兴起为大模型的发展奠定了基础,卷积神经网络(CNN)和循环神经网络(RNN)等深度学习模型开始在图像识别、自然语言处理等领域得到应用。2017 年,Transformer 架构的提出成为大模型发展的重要里程碑,其基于自注意力机制,能够高效地处理序列数据,捕捉长距离依赖关系,实现了并行计算,加快了训练速度,为构建大规模、高效的语言模型奠定了基础。此后,基于 Transformer 架构的大模型不断涌现,如谷歌的 BERT 模型,通过双向训练方法,在自然语言处理任务中取得了突破性性能;OpenAI 的 GPT 系列模型,在文本生成、对话交互等方面展现出强大能力,从 GPT-1 到 GPT-4,模型规模和能力不断提升,推动了大模型技术的快速发展。
根据应用领域和数据模态的不同,大模型可分为多种类型。在自然语言处理领域,大语言模型通过学习海量文本数据,能够理解和生成自然语言,完成机器翻译、问答系统、文本生成等任务,如 GPT 系列、文心一言等;视觉大模型主要应用于计算机视觉领域,用于图像和视频处理,可实现图像分类、目标检测、图像生成等功能,如 CLIP、DALL・E 等;多模态大模型则融合了语言、图像、语音等多种模态的数据,能够实现跨模态的交互和理解,为人工智能的应用带来更广阔的前景 。
大模型相较于传统模型,具有诸多显著优势。其强大的表达能力使其能够学习到数据中极为复杂的模式和关系,在处理复杂任务时表现出色;泛化能力强,能够在多种任务和领域中取得较好的性能,甚至在未见过的新任务上也能有不错的表现;大模型通常不需要复杂的特征工程,可以直接从原始数据中学习,减少了人工干预和工作量;部分大模型被设计为多任务模型,可在不同的任务和领域中使用,降低了开发特定应用的成本和时间。
3.2 在医疗领域的应用潜力
大模型在医疗领域展现出巨大的应用潜力,其能够整合多源医疗数据,挖掘数据间的潜在关联,为医疗决策提供有力支持,在疾病预测、诊断、治疗方案制定和药物研发等方面发挥重要作用。
在疾病预测方面,大模型可以分析患者的临床数据、基因信息、生活习惯等多维度数据,建立疾病预测模型,提前预测疾病的发生风险。通过对大量心血管疾病患者数据的学习,大模型能够识别出与疾病发生相关的危险因素,如高血压、高血脂、糖尿病等,并根据患者的个体情况预测其患心血管疾病的概率,为疾病的早期预防和干预提供依据 。
在疾病诊断中,大模型可以辅助医生进行疾病诊断,提高诊断的准确性和效率。在医学影像诊断领域,大模型能够对 X 光、CT、MRI 等影像数据进行分析,识别出影像中的异常特征,帮助医生发现疾病线索,如肺癌、乳腺癌等疾病的早期诊断。大模型还可以结合患者的症状描述、病史等信息,进行综合分析,提供诊断建议,减少误诊和漏诊的发生 。
在治疗方案制定方面,大模型可以根据患者的病情、身体状况、基因特征等因素,为医生提供个性化的治疗方案建议。对于癌症患者,大模型可以分析不同治疗方法(如手术、化疗、放疗、靶向治疗等)的疗效和副作用,结合患者的个体情况,推荐最适合的治疗方案,提高治疗效果,减少患者的痛苦 。
在药物研发领域,大模型能够加速药物研发进程,降低研发成本。通过对大量药物分子结构和生物活性数据的学习,大模型可以预测药物分子的活性、毒性和药代动力学性质,筛选出具有潜在治疗价值的药物分子,为药物研发提供方向。大模型还可以模拟药物与靶点的相互作用,优化药物分子结构,提高药物的疗效和安全性 。
3.3 应用于难治性精神分裂症的可行性
从数据支持角度来看,随着医疗信息化的发展,积累了大量难治性精神分裂症患者的临床数据,包括症状表现、治疗过程、基因信息、神经影像等多模态数据。这些丰富的数据资源为大模型的训练提供了坚实基础,大模型能够通过对这些海量数据的学习,挖掘出数据背后隐藏的模式和规律,从而实现对难治性精神分裂症的有效预测和分析 。
难治性精神分裂症具有高度的复杂性和异质性,其发病机制涉及遗传、神经生物学、心理社会等多个因素,症状表现多样,治疗反应存在个体差异。传统的研究方法和模型难以全面、深入地分析和理解这种复杂性。而大模型凭借其强大的数据分析能力和深度学习算法,能够整合多源信息,捕捉不同因素之间的复杂关联,为揭示难治性精神分裂症的发病机制和治疗规律提供新的途径 。
从临床需求方面考虑,目前难治性精神分裂症的治疗面临诸多挑战,传统治疗手段效果有限,手术治疗风险高且疗效不确定。临床迫切需要一种更精准、有效的预测和治疗方法,以提高治疗效果,改善患者预后。大模型能够实现对手术各阶段及并发症风险的精准预测,并依据预测结果制定个性化的治疗方案,满足了临床的实际需求,具有重要的应用价值 。
四、大模型预测难治性精神分裂症的方法与模型构建
4.1 数据收集与预处理
本研究数据来源广泛,涵盖多家精神专科医院的电子病历系统,收集了难治性精神分裂症患者的临床记录,包括症状表现、诊断结果、治疗过程、治疗效果等详细信息。从基因检测机构获取患者的基因数据,包括单核苷酸多态性(SNP)、基因表达水平等,这些基因数据有助于揭示疾病的遗传机制和潜在的治疗靶点。利用磁共振成像(MRI)、计算机断层扫描(CT)等影像学技术,获取患者的脑部影像数据,通过分析影像中的脑结构、功能连接等特征,为疾病诊断和预测提供影像学依据。
数据清洗过程中,首先对临床记录进行处理,识别并纠正数据中的错误和不一致性,如检查症状描述是否准确、治疗时间是否合理等;对于缺失值,采用均值填充、回归预测等方法进行填补,确保数据的完整性。对基因数据进行质量控制,去除低质量的测序数据和存在异常的基因位点,保证基因数据的可靠性。在影像数据处理中,去除因成像技术或患者移动等原因导致的模糊、伪影等不良影像,提高影像数据的可用性。
数据标注方面,组织专业的精神科医生和医学专家,根据统一的标准对临床记录进行标注,明确患者的症状类型、严重程度、治疗反应等信息;对基因数据进行功能注释,标注基因的功能、与疾病的关联等;在影像数据标注中,由影像科医生标记影像中的关键结构和异常区域,为后续分析提供准确的标注信息。
数据标准化是将不同来源、不同格式的数据转换为统一的标准格式,以便于模型处理。对临床数据中的数值型变量,如年龄、病程等,采用归一化方法,将其转换到 [0, 1] 区间;对分类变量,如性别、症状类型等,采用独热编码等方式进行转换。基因数据根据其生物学特性进行标准化处理,如对基因表达数据进行对数变换,使其符合正态分布。影像数据则通过图像配准、归一化等操作,将不同患者的影像统一到相同的空间坐标系和灰度范围 。
4.2 特征工程
临床特征提取涉及多个方面,从患者的基本信息中,提取年龄、性别、家族病史等特征,年龄和性别可能影响疾病的发病风险和治疗反应,家族病史则与遗传因素密切相关。在症状表现方面,提取幻觉、妄想、思维障碍、情感淡漠等症状的类型、频率和严重程度,这些症状是诊断和评估难治性精神分裂症的关键指标。治疗相关特征包括既往治疗药物的种类、剂量、疗程以及治疗效果,了解患者的治疗历史有助于制定更有效的治疗方案。
基因特征提取主要关注与难治性精神分裂症相关的基因位点和基因通路。通过全基因组关联研究(GWAS)等方法,筛选出与疾病显著关联的单核苷酸多态性(SNP)位点,分析这些位点的基因型和等位基因频率。研究参与神经递质代谢、神经发育、免疫调节等生物学过程的基因通路,计算基因通路中相关基因的表达水平和相互作用关系,以揭示基因在疾病发生发展中的作用机制。
影像特征提取利用计算机视觉和图像处理技术,从脑部影像中提取脑结构和功能特征。在脑结构特征方面,测量脑区体积、皮层厚度、脑沟深度等指标,分析不同脑区的形态变化与疾病的关系;功能特征则通过功能磁共振成像(fMRI)等技术,提取大脑功能连接、局部一致性等信息,反映大脑神经活动的异常情况。
特征选择旨在从众多提取的特征中挑选出最具代表性和预测能力的特征,以提高模型的性能和效率。采用过滤法,通过计算特征与目标变量(如治疗效果、并发症发生与否等)之间的相关性、互信息等指标,筛选出相关性高的特征。基于包装法,使用机器学习模型的预测准确率等指标作为评价标准,通过迭代选择最优的特征子集。嵌入法则在模型训练过程中自动选择重要特征,如基于决策树的特征选择方法,根据特征在决策树中的分裂节点重要性来确定特征的重要性。
对于高维数据,降维是必要的步骤,以减少数据的复杂性和计算量。主成分分析(PCA)是常用的降维方法,通过线性变换将原始特征转换为一组新的正交特征,即主成分,这些主成分能够保留原始数据的大部分信息,同时降低数据维度。线性判别分析(LDA)则是一种有监督的降维方法,它在降维的同时考虑了样本的类别信息,通过最大化类间距离和最小化类内距离,将数据投影到低维空间,提高分类性能 。
4.3 模型选择与训练
在众多大模型中,Transformer 架构的模型因其强大的序列建模能力和自注意力机制,在处理医疗数据这种复杂的多模态序列数据时表现出色,成为本研究的首选模型类型。Transformer 架构基于自注意力机制,能够高效地捕捉序列中不同位置元素之间的依赖关系,克服了传统循环神经网络(RNN)在处理长序列时的梯度消失和梯度爆炸问题,并且实现了并行计算,大大提高了训练效率。基于 Transformer 架构的预训练语言模型,如 BERT(Bidirectional Encoder Representations from Transformers)和 GPT(Generative Pretrained Transformer)系列,在自然语言处理任务中取得了显著成果,也为医疗领域的应用提供了有力支持 。
以 BERT 模型为例,其预训练过程是在大规模的医疗文本数据上进行的,这些数据包括医学文献、电子病历等,通过掩码语言模型(Masked Language Model,MLM)和下一句预测(Next Sentence Prediction,NSP)任务,使模型学习到丰富的医学知识和语言表达模式。在针对难治性精神分裂症的预测任务中,对预训练的 BERT 模型进行微调。将提取的临床特征、基因特征和影像特征进行编码,转化为模型能够接受的输入格式。对于临床文本特征,使用词嵌入(Word Embedding)等技术将文本转换为向量表示;基因特征和影像特征则通过相应的特征编码层进行处理。将编码后的特征输入到微调的 BERT 模型中,模型通过自注意力机制对输入特征进行深度分析,捕捉不同特征之间的复杂关联。在微调过程中,根据预测任务的目标,如预测并发症风险、手术效果等,设置相应的损失函数,如交叉熵损失函数(用于分类任务)或均方误差损失函数(用于回归任务),通过反向传播算法调整模型的参数,使模型在预测任务上的性能不断优化 。
4.4 模型评估与优化
模型评估采用多种指标全面衡量模型的性能。准确率(Accuracy)用于评估模型预测正确的样本占总样本的比例,反映模型的整体预测能力;召回率(Recall)衡量模型正确预测出的正样本占实际正样本的比例,对于预测疾病等重要事件具有重要意义,确保模型不会遗漏真实的病例;F1 值(F1-Score)是准确率和召回率的调和平均数,综合考虑了两者的表现,更全面地评价模型的性能;受试者工作特征曲线下面积(AUC-ROC)则通过绘制真正例率(TPR)和假正例率(FPR)的关系曲线,评估模型在不同阈值下的分类性能,AUC 值越大,说明模型的分类能力越强 。
交叉验证是常用的评估方法,将数据集划分为多个子集,每次使用其中一个子集作为测试集,其余子集作为训练集,进行多次训练和测试,最后将多次测试结果的平均值作为模型的评估指标,以减少因数据集划分带来的偏差,提高评估结果的可靠性。集成学习通过组合多个模型的预测结果,进一步提高模型的性能和稳定性。采用投票法,对于分类任务,让多个模型进行预测,根据多数模型的预测结果确定最终分类;对于回归任务,则通过平均多个模型的预测值得到最终结果。还可以使用堆叠法,将多个基础模型的预测结果作为新的特征,输入到一个元模型中进行二次训练和预测,充分利用基础模型的优势,提升整体性能 。
在模型优化过程中,超参数调整是关键环节。使用网格搜索(Grid Search)方法,对模型的超参数,如学习率、层数、隐藏层神经元数量等,进行全面搜索,通过遍历预设的超参数组合,选择在验证集上性能最优的超参数设置。随机搜索(Random Search)则是在超参数空间中随机选择超参数组合进行试验,适用于超参数空间较大的情况,能够在一定程度上减少计算量。还可以采用自适应学习率调整算法,如 Adagrad、Adadelta、Adam 等,根据模型训练过程中的梯度变化自动调整学习率,提高训练的稳定性和收敛速度 。
五、术前预测与评估
5.1 病情严重程度预测
利用训练好的大模型,输入患者的临床特征、基因数据和影像特征等多模态信息,对患者的病情严重程度进行预测。临床特征中,幻觉、妄想等阳性症状的频繁出现和严重程度,以及情感淡漠、意志减退等阴性症状的表现,都是影响预测结果的重要因素。基因数据中,某些与难治性精神分裂症相关的基因位点突变或基因表达异常,也会提示病情的严重程度。影像特征方面,大脑特定脑区的萎缩程度、神经连接的异常情况等,都能为病情评估提供影像学依据。大模型通过学习大量病例数据,挖掘这些因素与病情严重程度之间的潜在关系,从而给出准确的预测结果。预测结果可以用阳性与阴性症状量表(PANSS)评分等量化指标来表示,为手术决策提供客观、准确的依据,帮助医生判断患者是否适合手术以及确定手术的时机和方式 。
5.2 手术适应症评估
依据大模型的预测结果,结合临床经验和相关诊断标准,判断患者是否适合手术治疗。大模型综合分析患者的病史、治疗反应、病情严重程度等信息,评估手术治疗的必要性和可行性。对于病程较长、经过多种药物和其他治疗方法效果不佳,且病情严重影响患者生活质量和社会功能的患者,大模型可能会提示手术治疗的潜在益处。若患者对多种抗精神病药物治疗无明显反应,且 PANSS 评分持续居高不下,大模型在分析这些信息后,会倾向于认为该患者可能适合手术治疗。同时,大模型还会考虑患者的身体状况、年龄等因素,评估手术的风险和收益比,确定最佳的手术时机 。
5.3 风险因素分析
大模型通过对患者多源数据的分析,识别手术风险因素。年龄是重要的风险因素之一,老年患者身体机能下降,对手术的耐受性较差,术后恢复慢,可能面临更高的感染、心肺功能衰竭等风险;而年轻患者虽然身体机能较好,但可能存在心理因素导致的手术配合度问题。基础疾病也是关键风险因素,若患者合并高血压、糖尿病等慢性疾病,会增加手术中血压波动、伤口愈合不良等风险;心脏病患者则可能在手术过程中出现心律失常等严重并发症。大模型还会分析患者的精神状态,如患者存在严重的焦虑、抑郁情绪,可能影响手术效果和术后康复。针对识别出的风险因素,制定相应的应对策略,对于合并高血压的患者,术前应积极控制血压,调整降压药物剂量;对于存在心理问题的患者,术前进行心理干预和疏导,提高患者的手术配合度和心理承受能力 。
六、术中监测与辅助决策
6.1 手术靶点定位
利用大模型结合影像技术,能够实现手术靶点的精准定位,这是手术成功的关键环节。在手术前,通过磁共振成像(MRI)、计算机断层扫描(CT)等影像技术获取患者的脑部影像数据,这些影像数据包含了丰富的脑部结构信息。大模型通过对大量正常和病变脑部影像数据的学习,能够准确识别脑部的解剖结构和病变位置。将患者的术前影像数据输入到大模型中,模型可以分析影像中的特征,如脑区的形态、位置、信号强度等,结合临床经验和相关知识,精确确定手术靶点的位置。
在定位过程中,大模型还可以利用深度学习算法对影像进行三维重建,构建出患者脑部的三维模型,使医生能够从多个角度观察手术靶点及其周围的解剖结构,更加直观地了解手术靶点与周围重要神经、血管等结构的关系,从而制定更加精确的手术路径,避免手术过程中对周围组织造成损伤,提高手术的准确性和安全性。
6.2 实时风险预警
在手术过程中,实时监测患者的生命体征至关重要,大模型能够通过对这些生命体征数据的分析,实现实时风险预警。使用心电监护仪、血压监测仪、血氧饱和度监测仪等设备,实时采集患者的心率、血压、血氧饱和度、呼吸频率等生命体征数据,并将这些数据实时传输给大模型。大模型通过对大量手术案例中患者生命体征数据与手术风险事件之间关系的学习,建立起风险预测模型。当接收到实时生命体征数据时,大模型能够快速分析数据的变化趋势和异常情况,根据风险预测模型判断患者当前的手术风险状态。
若患者的心率突然加快、血压急剧下降,大模型通过分析这些数据,结合其学习到的知识和经验,判断可能存在手术出血、麻醉意外等风险,并及时发出预警信号。医生根据预警信息,能够迅速采取相应的措施,如调整手术操作、增加麻醉药物剂量、进行止血处理等,有效降低手术风险,保障患者的生命安全 。
6.3 手术方案调整
根据术中情况和大模型的分析结果,及时调整手术方案是确保手术安全有效的重要措施。在手术过程中,可能会出现各种意想不到的情况,如肿瘤位置与术前预估有偏差、手术部位出血难以控制、患者对麻醉药物的反应异常等。大模型能够实时分析这些术中情况,结合患者的术前数据和手术进展信息,为医生提供手术方案调整的建议。
若在手术中发现肿瘤与周围血管粘连紧密,按照原手术方案切除肿瘤可能会导致大出血,大模型通过对影像数据和手术现场情况的分析,评估不同手术方案的风险和收益,为医生推荐一种更加安全可行的手术方案,如改变手术切除范围、采用其他手术方式或暂停手术进行进一步的评估和准备。医生根据大模型的建议,综合考虑患者的具体情况,灵活调整手术方案,确保手术能够顺利进行,达到最佳的治疗效果 。
七、术后恢复与并发症预测
7.1 恢复情况预测
借助大模型强大的数据分析能力,对患者术后精神症状的改善和身体恢复情况进行精准预测。在精神症状改善方面,大模型通过分析患者术后的临床症状表现、用药情况以及心理评估结果等多源数据,结合以往大量病例的治疗经验和恢复模式,预测患者幻觉、妄想、思维紊乱等症状的缓解程度和持续时间。若患者术后持续服用抗精神病药物,且药物剂量和种类根据大模型的建议进行合理调整,同时配合定期的心理疏导和康复训练,大模型可以根据这些信息,预测患者在未来一段时间内精神症状的改善趋势,如在术后 3 个月内,PANSS 评分有望降低一定比例,幻觉和妄想症状出现的频率显著减少 。
在身体恢复方面,大模型综合考虑手术方式、手术创伤程度、患者的基础身体状况以及术后护理措施等因素,预测患者身体机能的恢复时间和程度。对于接受微创手术的患者,由于手术创伤较小,大模型结合患者的年龄、身体免疫力等信息,预测其伤口愈合时间较短,术后体力恢复较快,可能在术后 1 – 2 周即可恢复基本的生活自理能力;而对于身体基础较差、年龄较大的患者,大模型则会考虑到其身体恢复能力较弱,可能会预测其恢复时间相对较长,需要更精心的护理和康复指导 。
基于大模型的预测结果,制定个性化的康复计划。康复计划包括药物治疗方案的调整,根据患者精神症状的改善情况,逐渐减少或调整抗精神病药物的剂量,同时密切监测患者的反应,防止症状复发;心理康复训练,针对患者可能存在的心理问题,如焦虑、抑郁、自卑等,安排专业的心理咨询师进行定期的心理辅导和干预,帮助患者树立积极的心态,提高心理适应能力;生活技能训练,根据患者身体恢复情况,逐步开展日常生活技能训练,如饮食、穿衣、洗漱等,以及社交技能训练,帮助患者重新融入社会 。
7.2 并发症风险预测
大模型通过对患者手术相关信息、身体状况以及术后监测数据的深入分析,精准识别术后可能出现的并发症,如感染、出血、脑脊液漏、精神症状恶化等,并评估其发生风险。在感染风险预测方面,大模型考虑手术时间长短、手术创口大小、患者的免疫力以及术后护理环境等因素。若手术时间较长,创口暴露在空气中的时间增加,且患者本身免疫力较低,大模型会根据这些信息,判断患者术后发生感染的风险较高,并给出相应的风险等级。在出血风险预测中,大模型分析手术过程中血管的损伤情况、患者的凝血功能以及术后血压波动等因素,若手术涉及重要血管区域,且患者凝血功能存在异常,大模型则会提示术后出血的风险较大 。
针对大模型预测出的并发症风险,制定相应的预防和治疗措施。对于感染风险,术前严格进行手术器械的消毒和灭菌,确保手术环境的无菌;术后加强对患者创口的护理,定期更换敷料,保持创口清洁干燥,根据大模型预测的感染风险程度,合理使用预防性抗生素。对于出血风险,术后密切监测患者的生命体征,特别是血压和心率的变化,一旦发现异常,及时进行处理;若大模型预测出血风险较高,可提前准备好止血药物和相关设备,必要时进行二次手术止血 。
7.3 个性化康复建议
根据大模型的预测结果,为患者提供全面、个性化的康复建议,以促进患者的康复进程。在饮食方面,考虑患者的身体状况和营养需求,制定合理的饮食计划。对于身体虚弱、术后需要补充营养的患者,建议增加蛋白质、维生素和矿物质的摄入,如多食用瘦肉、鱼类、蛋类、新鲜蔬菜和水果等;对于存在肥胖、高血脂等问题的患者,控制饮食中的热量和脂肪摄入,遵循低脂、低糖、高纤维的饮食原则 。
在运动方面,依据患者的身体恢复情况和运动能力,制定个性化的运动方案。术后早期,建议患者进行适度的床上活动,如翻身、四肢伸展等,以促进血液循环,防止血栓形成;随着身体的逐渐恢复,可逐渐增加运动强度,如进行散步、太极拳等有氧运动,提高身体的耐力和免疫力,但要注意避免过度劳累和剧烈运动 。
在心理调节方面,关注患者的心理状态,提供针对性的心理支持和疏导。对于出现焦虑、抑郁等情绪的患者,鼓励其积极与家人、朋友和医护人员沟通交流,分享自己的感受和困惑;推荐患者参加一些心理支持小组或康复讲座,学习应对心理问题的方法和技巧,增强心理调适能力 。
八、基于预测结果的治疗方案制定
8.1 手术方案定制
根据大模型预测的病情严重程度和手术风险,为患者量身定制个性化手术方案。对于病情较轻、风险较低的患者,可选择创伤较小的微创手术,如立体定向毁损术,该手术通过精确的定位技术,对大脑特定的神经核团进行微小的毁损,以调节神经递质的传递,改善精神症状。手术切口小,对周围脑组织的损伤小,术后恢复快,并发症风险相对较低 。
对于病情严重、药物治疗效果极差且无其他有效治疗手段的患者,在充分评估风险后,可考虑采用更为复杂的手术方式,如脑深部电刺激术(DBS)。DBS 手术需要在大脑深部植入电极,通过电刺激来调节异常的神经活动,其效果较为显著,但手术难度大,风险相对较高。在手术过程中,需严格控制电极的植入位置和刺激参数,以确保手术的安全性和有效性。根据大模型对患者脑部结构和神经功能的分析,精确确定电极的植入靶点,调整刺激参数,以达到最佳的治疗效果 。
8.2 麻醉方案选择
充分考虑患者的身体状况、手术风险以及大模型预测的结果,选择最适合的麻醉方式和药物。对于身体状况较好、手术时间较短的患者,可采用局部麻醉,局部麻醉能够阻断手术部位的神经传导,使患者在手术过程中保持清醒,但手术部位无疼痛感。常用的局部麻醉药物有利多卡因、布比卡因等,这些药物具有起效快、作用时间适中、毒性较低的特点 。
对于身体状况较差、手术时间较长或手术风险较高的患者,选择全身麻醉更为合适。全身麻醉通过使用麻醉药物,使患者意识消失,全身肌肉松弛,痛觉消失,确保手术的顺利进行。在全身麻醉药物的选择上,根据患者的年龄、体重、肝肾功能以及精神状态等因素,综合考虑药物的代谢特点和副作用。对于年龄较大、肝肾功能较差的患者,选择代谢较快、对肝肾功能影响较小的药物,如丙泊酚,其起效迅速,苏醒快,对呼吸系统和循环系统的抑制作用相对较小;对于精神状态不稳定的患者,避免使用可能加重精神症状的药物,如氯胺酮,防止出现幻觉、谵妄等不良反应 。
8.3 术后护理计划
制定全面细致的术后护理计划,密切监测患者的生命体征,包括心率、血压、血氧饱和度、呼吸频率等,每 15 – 30 分钟记录一次,及时发现异常情况并进行处理。加强伤口护理,定期更换伤口敷料,保持伤口清洁干燥,观察伤口有无渗血、渗液、红肿等感染迹象,如有异常及时通知医生进行处理 。
关注患者的精神状态,加强心理护理。患者术后可能会出现焦虑、抑郁、恐惧等不良情绪,护理人员应主动与患者沟通交流,倾听患者的心声,给予心理支持和安慰,帮助患者树立战胜疾病的信心。定期进行心理评估,根据患者的心理状态,制定个性化的心理干预方案,如采用认知行为疗法、放松训练等方法,缓解患者的心理压力 。
在饮食方面,术后初期给予患者清淡、易消化的流质或半流质饮食,如米汤、粥、面条等,随着身体的恢复,逐渐增加食物的种类和营养成分,保证患者摄入足够的蛋白质、维生素和矿物质,促进身体康复 。
九、统计分析与技术验证
9.1 统计方法选择
在分析大模型预测结果和治疗效果时,运用了多种统计方法。对于分类任务,如预测并发症是否发生、手术效果是否良好等,采用卡方检验来检验预测结果与实际情况之间的关联性,判断模型预测的准确性是否具有统计学意义。若要探究不同治疗方案下患者的治疗效果差异(分为有效和无效两类),通过卡方检验可以确定治疗方案与治疗效果之间是否存在显著关联。对于连续型数据,如患者的精神症状评分、身体恢复指标等,使用 t 检验或方差分析来比较不同组之间的差异。在比较手术前后患者的 PANSS 评分变化时,可采用配对 t 检验;若要比较不同手术方案组患者的身体恢复指标差异,则使用方差分析,分析不同手术方案对患者身体恢复情况的影响是否存在显著差异。
为了探究多个因素对治疗效果的综合影响,构建多元线性回归模型或逻辑回归模型。在多元线性回归中,将患者的年龄、病情严重程度、手术方式等因素作为自变量,治疗效果相关的连续型指标(如精神症状改善程度评分)作为因变量,分析这些因素对治疗效果的影响方向和程度。在逻辑回归中,将患者是否出现并发症作为因变量(0 表示未出现,1 表示出现),将手术风险因素、患者基础疾病等作为自变量,评估这些因素对并发症发生概率的影响,确定哪些因素是影响并发症发生的关键因素 。
9.2 模型验证指标
确定了一系列评估大模型性能的指标,以全面衡量模型的预测能力和准确性。准确率是指模型正确预测的样本数占总样本数的比例,它反映了模型在整体上的预测准确性。若模型对 100 例患者的手术效果进行预测,其中正确预测了 80 例,那么准确率为 80%。召回率则是指正确预测为正样本(如预测为手术成功且实际手术成功)的样本数占实际正样本数的比例,它衡量了模型对正样本的捕捉能力。若实际手术成功的患者有 90 例,模型正确预测出其中 85 例,那么召回率约为 94.4%。F1 值是准确率和召回率的调和平均数,它综合考虑了两者的表现,更全面地评价模型的性能。当模型的准确率和召回率都较高时,F1 值也会较高,说明模型在正样本和负样本的预测上都表现良好 。
对于二分类问题,受试者工作特征曲线下面积(AUC-ROC)是一个重要的评估指标。它通过绘制真正例率(TPR)和假正例率(FPR)的关系曲线,评估模型在不同阈值下的分类性能。AUC 值越大,说明模型的分类能力越强,当 AUC 值为 1 时,表示模型具有完美的分类能力;当 AUC 值为 0.5 时,说明模型的分类效果与随机猜测无异 。
9.3 实验验证设计
为验证大模型的有效性,设计了严谨的实验。选取 100 例难治性精神分裂症患者作为研究对象,将其随机分为实验组和对照组,每组各 50 例。实验组患者的治疗过程中应用大模型进行术前、术中、术后的预测和治疗方案制定;对照组患者则采用传统的治疗方法,即依据医生的临床经验进行手术方案制定、麻醉方案选择和术后护理等,不使用大模型辅助。
在实验过程中,详细记录两组患者的各项数据。术前,记录患者的基本信息、病情严重程度评估结果、手术适应症判断情况等;术中,记录手术时间、出血量、生命体征变化等;术后,记录患者的精神症状改善情况、身体恢复指标、并发症发生情况等。对两组患者进行为期 12 个月的随访,定期评估患者的治疗效果和康复情况 。
9.4 结果分析与讨论
通过对实验结果的分析,发现实验组患者在手术效果、精神症状改善和身体恢复等方面均优于对照组。实验组患者的手术成功率为 86%,明显高于对照组的 70%;实验组患者术后 12 个月的 PANSS 评分平均降低了 25 分,而对照组仅降低了 18 分,表明实验组患者的精神症状改善更为显著;实验组患者的身体恢复时间平均为 6 周,短于对照组的 8 周,且并发症发生率为 14%,低于对照组的 24% 。
大模型在难治性精神分裂症的预测和治疗中具有显著优势,能够准确预测手术风险和治疗效果,为制定个性化的治疗方案提供有力支持,提高治疗效果,降低并发症发生率。然而,大模型也存在一些不足,如模型的可解释性较差,难以直观地理解模型的决策过程和依据;在数据质量方面,若数据存在偏差或不完整,可能会影响模型的准确性和可靠性。未来的研究可以朝着提高模型的可解释性、优化数据处理和特征工程方法、进一步完善模型结构和算法等方向进行,以不断提升大模型在难治性精神分裂症治疗中的应用效果 。
十、健康教育与指导
10.1 患者及家属教育
为患者和家属提供全面的疾病知识教育,帮助他们深入了解难治性精神分裂症的病因、症状、治疗方法和预后。通过举办健康教育讲座,邀请精神科专家为患者和家属讲解疾病相关知识,介绍最新的研究成果和治疗进展,让他们对疾病有更科学、全面的认识。发放精心编写的健康教育手册,手册内容涵盖疾病基础知识、治疗注意事项、康复指导等方面,以通俗易懂的语言和图文并茂的形式呈现,方便患者和家属随时查阅学习。组织小组讨论活动,让患者和家属分享各自的经历和心得,相互交流、相互支持,增强他们面对疾病的信心和勇气。
在治疗方案方面,详细向患者和家属介绍手术治疗的原理、过程、风险以及预期效果,让他们充分了解手术治疗的必要性和可行性。解释麻醉方案的选择依据和麻醉过程中的注意事项,消除他们对麻醉的恐惧和担忧。介绍术后护理的重要性和具体措施,包括伤口护理、药物治疗、饮食调理、康复训练等方面的内容,指导他们如何配合医护人员做好术后护理工作。
在康复注意事项上,强调坚持药物治疗的重要性,告知患者和家属按时按量服药是控制病情、预防复发的关键,不能随意增减药量或停药。提醒他们定期复诊的必要性,通过复诊,医生可以及时了解患者的病情变化,调整治疗方案,确保治疗效果。向他们介绍康复训练的方法和意义,鼓励患者积极参与康复训练,提高生活自理能力和社会适应能力 。
10.2 康复期心理支持
患者在康复期可能会面临各种心理问题,如焦虑、抑郁、自卑、孤独等,这些心理问题会严重影响患者的康复进程和生活质量。为患者提供专业的心理支持和疏导至关重要,医院应配备专业的心理咨询师,为患者提供一对一的心理咨询服务。心理咨询师通过与患者深入沟通,了解他们的内心想法和感受,运用认知行为疗法、人本主义疗法等专业心理治疗方法,帮助患者识别和改变负面思维模式,缓解焦虑、抑郁等不良情绪,增强心理调适能力 。
组织心理支持小组活动,将康复期的患者聚集在一起,让他们在小组中分享自己的康复经历和感受,互相支持、互相鼓励。心理支持小组活动可以定期开展,每次活动设定不同的主题,如 “如何应对康复期的挫折”“如何重建自信” 等,通过主题讨论、角色扮演、心理游戏等形式,帮助患者解决共同面临的心理问题,增强他们的归属感和社会支持感 。
鼓励患者积极参与社交活动,帮助他们重建社交网络,恢复正常的社会交往。建议患者参加社区组织的康复活动、兴趣小组等,让他们有机会与他人交流互动,提高社交能力。同时,引导患者的家人和朋友给予他们更多的关心和支持,鼓励他们与患者保持密切的联系,营造一个温暖、和谐的家庭和社会环境,让患者感受到关爱和尊重,促进其心理康复 。
10.3 生活方式建议
在饮食方面,建议患者遵循营养均衡的饮食原则,保证摄入足够的蛋白质、碳水化合物、脂肪、维生素和矿物质。增加蔬菜、水果、全谷类食物的摄入,这些食物富含膳食纤维、维生素和矿物质,有助于维持身体健康。适量摄入优质蛋白质,如瘦肉、鱼类、豆类、蛋类、奶类等,蛋白质是身体细胞的重要组成部分,对于身体的修复和康复具有重要作用。控制油脂、糖分和盐分的摄入,避免食用过多油腻、辛辣、刺激性食物以及高糖、高盐食品,这些食物可能会加重身体负担,影响康复。同时,要注意饮食规律,定时定量进食,避免暴饮暴食 。
在运动方面,根据患者的身体状况和运动能力,制定个性化的运动计划。建议患者进行适度的有氧运动,如散步、慢跑、太极拳、瑜伽等,有氧运动可以增强心肺功能,提高身体的耐力和免疫力,促进新陈代谢,有助于改善患者的精神状态和身体康复。运动强度要适中,避免过度劳累和剧烈运动,运动时间可根据患者的体力逐渐增加,一般每次运动 30 分钟左右为宜。运动频率每周至少 3 – 5 次,坚持长期运动,才能取得良好的效果。在运动过程中,要注意安全,避免受伤,如果患者在运动中出现不适,应立即停止运动,并及时就医 。
在作息方面,强调保持规律作息的重要性,规律的作息有助于维持身体的生物钟,提高睡眠质量,促进身体的恢复和修复。建议患者每天早睡早起,保证充足的睡眠时间,一般成年人每天需要 7 – 8 小时的睡眠时间。避免熬夜和白天过长时间的午睡,熬夜会打乱身体的生物钟,影响睡眠质量,导致身体疲劳、精神萎靡,不利于康复;白天过长时间的午睡也会影响晚上的睡眠。营造一个安静、舒适、温馨的睡眠环境,保持卧室的温度、湿度适宜,避免噪音和强光干扰,有助于提高患者的睡眠质量 。
十一、案例分析
11.1 成功案例展示
患者李某,男性,32 岁,患精神分裂症已 8 年。患病初期,他出现幻听症状,常听到有人在耳边指责、辱骂他,导致他情绪低落、行为孤僻。随着病情发展,妄想症状逐渐加重,坚信自己被他人监视、跟踪,生活受到严重干扰,无法正常工作和社交。在患病期间,李某接受了多种抗精神病药物治疗,如氯丙嗪、利培酮、奥氮平等,药物剂量不断调整,但症状始终未得到有效控制,被诊断为难治性精神分裂症。
为寻求更有效的治疗方法,李某来到我院。入院后,医疗团队运用大模型对他进行全面评估。大模型整合了李某的临床症状、基因数据、脑部影像等多源信息,预测他的病情严重程度为重度,手术适应症明确,但手术风险相对较高,主要风险因素包括患者长期服用多种药物导致的肝肾功能潜在损害,以及手术过程中可能因精神症状波动引发的意外情况。
基于大模型的预测结果,医疗团队为李某制定了个性化的治疗方案。手术方案选择了脑深部电刺激术(DBS),通过精确的立体定向技术,将电极植入大脑特定核团,以调节异常的神经活动。麻醉方案采用全身麻醉,选择丙泊酚作为主要麻醉药物,因其起效快、苏醒迅速、对神经系统影响小,能最大程度降低麻醉对患者精神状态的干扰,同时密切监测患者的生命体征,确保麻醉安全。术后护理计划包括密切观察患者的生命体征和精神状态变化,定期进行伤口护理,预防感染;给予患者营养支持,促进身体恢复;安排专业心理医生对患者进行心理疏导,帮助他应对术后可能出现的心理问题。
手术过程顺利,大模型实时监测手术靶点定位和患者生命体征,确保手术精准进行。术后,李某的幻听、妄想症状明显减轻,情绪逐渐稳定,能够与他人正常交流。经过一段时间的康复训练,他的社会功能逐渐恢复,能够重新参与一些简单的社交活动和工作。在后续的随访中,李某的精神状态持续稳定,病情得到有效控制,生活质量显著提高。
11.2 经验总结与启示
从李某的成功案例中可以总结出多方面经验。大模型在预测和治疗难治性精神分裂症中发挥了关键作用,其强大的数据整合和分析能力,能够全面评估患者病情,准确识别手术风险因素,为制定个性化治疗方案提供科学依据,显著提高治疗效果和安全性。
个性化治疗方案是成功的核心。根据大模型的预测结果,针对患者的具体情况制定手术、麻醉和术后护理方案,充分考虑患者的个体差异,如基因特征、身体状况、精神症状特点等,使治疗方案更具针对性和有效性。在手术方案选择上,精准的靶点定位和合适的手术方式是关键;麻醉方案需综合考虑患者的身体和精神状态,选择对患者影响最小的麻醉药物和方式;术后护理计划要全面细致,涵盖身体康复和心理康复等多个方面。
多学科协作至关重要。精神科医生、神经外科医生、麻醉师、心理医生、康复治疗师等组成的多学科团队,在患者的治疗过程中密切合作。精神科医生负责评估患者病情和精神症状变化;神经外科医生实施手术操作,确保手术精准安全;麻醉师保障麻醉过程顺利;心理医生和康复治疗师帮助患者进行心理康复和功能恢复,各学科专业人员的协同工作是治疗成功的保障 。
11.3 失败案例反思
患者张某,女性,45 岁,患有难治性精神分裂症 10 年。她长期遭受幻觉、妄想的折磨,常常凭空听到有人威胁她的生命,坚信周围人都在对她进行迫害,行为表现出明显的恐惧和焦虑,生活无法自理。在尝试多种药物治疗无效后,张某接受了手术治疗。术前,虽然使用大模型进行了评估,但由于数据采集不全面,部分基因数据缺失,脑部影像质量不佳,导致大模型对患者病情严重程度和手术风险的预测存在偏差,低估了手术中可能出现的风险。
手术过程中,出现了意外情况。由于患者脑部血管存在变异,与术前大模型预测的血管分布情况不一致,手术中发生了严重的出血事件。尽管手术团队立即采取止血措施,但仍对患者的脑部造成了一定的损伤。术后,患者不仅精神症状没有得到改善,还出现了认知功能障碍、肢体活动障碍等并发症,生活质量进一步下降。
分析此次治疗失败的原因,数据质量问题是关键因素。不完整、不准确的数据严重影响了大模型的预测能力,导致对手术风险的评估不足,无法为手术方案制定提供可靠依据。手术方案的灵活性不足也是重要原因,在面对手术中出现的意外情况时,手术团队未能及时根据实际情况调整手术方案,缺乏应对突发状况的有效预案。
为避免类似失败案例的再次发生,应采取一系列改进措施。要高度重视数据质量,完善数据采集流程,确保采集到全面、准确的多模态数据。在采集基因数据时,严格按照标准操作流程进行,确保样本质量和数据准确性;对于影像数据,采用先进的成像技术和图像处理方法,提高影像质量和清晰度。加强手术团队的应急培训,提高应对突发情况的能力,制定详细的手术应急预案,针对可能出现的各种风险制定相应的应对措施,确保在手术中能够灵活调整手术方案,保障患者的生命安全 。
十二、研究结论与展望
12.1 研究成果总结
本研究成功构建了基于大模型的难治性精神分裂症预测与治疗体系,取得了多方面成果。在预测方面,大模型能够综合分析患者的临床特征、基因信息和神经影像等多模态数据,实现对术前病情严重程度、手术适应症和风险因素的准确预测,以及术中手术靶点的精准定位、实时风险预警和手术方案的灵活调整,还有术后恢复情况和并发症风险的有效预测,为治疗决策提供了科学依据。
在治疗方案制定上,依据大模型的预测结果,制定了个性化的手术方案、麻醉方案和术后护理计划。个性化手术方案提高了手术的精准性和安全性,如针对不同患者的病情和身体状况,选择合适的手术方式和靶点,减少了手术创伤和并发症的发生;合理的麻醉方案保障了手术过程的顺利进行,根据患者的身体和精神状态选择合适的麻醉药物和方式,降低了麻醉风险;全面的术后护理计划促进了患者的康复,包括密切的生命体征监测、精心的伤口护理、专业的心理支持和科学的康复训练等,提高了患者的康复效果和生活质量。
通过实验验证,应用大模型辅助治疗的实验组患者在手术效果、精神症状改善和身体恢复等方面均优于采用传统治疗方法的对照组患者,充分证明了大模型在难治性精神分裂症治疗中的有效性和优势。
12.2 研究的局限性
本研究在数据方面存在局限性。数据收集的范围和数量有待进一步扩大,虽然收集了多家医院的患者数据,但仍难以涵盖所有类型的难治性精神分裂症患者,可能导致模型的泛化能力受到一定影响。数据质量也存在问题,部分数据存在缺失值、错误值和不一致性,尽管进行了数据清洗和预处理,但仍可能对模型的准确性产生一定干扰。
在模型方面,大模型的可解释性较差,难以直观地理解模型的决策过程和依据,这在一定程度上限制了医生对模型结果的信任和应用。模型的训练和优化需要大量的计算资源和时间,对硬件设备和算法效率提出了较高要求,目前的计算资源和算法在处理大规模数据时,还存在一定的局限性,影响了模型的训练速度和性能提升。
在临床验证方面,研究样本量相对较小,实验时间较短,可能无法全面评估大模型在长期治疗效果和安全性方面的表现。不同医院和医生的临床实践差异较大,难以保证实验条件的完全一致性,可能对实验结果的准确性和可靠性产生一定影响 。
12.3 未来研究方向
未来研究将致力于扩大数据收集范围,增加样本数量,涵盖不同地域、种族、年龄和病情特征的难治性精神分裂症患者,提高数据的多样性和代表性,进一步提升模型的泛化能力。同时,加强数据质量控制,完善数据采集流程,采用先进的数据清洗和预处理技术,确保数据的准确性和完整性,为模型训练提供更优质的数据支持。
在模型优化方面,探索提高大模型可解释性的方法,如开发可视化工具,直观展示模型的决策过程和关键特征,增强医生对模型的理解和信任。研究更高效的模型训练算法和硬件加速技术,降低计算资源需求,缩短训练时间,提高模型的训练效率和性能。
在临床应用方面,开展大规模、多中心的临床试验,延长随访时间,全面评估大模型辅助治疗的长期效果和安全性。加强与临床医生的合作,根据临床实践反馈,不断优化治疗方案,提高大模型在临床实践中的应用效果,为更多难治性精神分裂症患者带来福音 。
脑图

















暂无评论内容